钠怎么家中制取

氯化钠电解需要801摄氏度融化,在家根本办不到,建议放弃。钠是一种金属元素,在周期表中位于第3周期、第ⅠA族,是碱金属元素的代表,质地柔软,能与水反应生成氢氧化钠,放出氢气,化学性质较活泼。
钠为银白色立方体结构金属,质软而轻可用小刀切割,密度比水小,为0.97g/cm3,熔点97.81℃,沸点882.9℃。新切面有银白色光泽,在空气中氧化转变为暗灰色,具有抗腐蚀性。钠是热和电的良导体,具有较好的导磁性,钾钠合金(液态)是核反应堆导热剂。
制取钠单质的化学方程式
具体如下:
第一种:电解熔融氢氧化钠,有三种选择。可以镍坩埚和铁电极。或者陶瓷坩埚和石墨电极,再或者陶瓷坩埚和一个石墨电极,一个铁电极。这三种方法最好。用酒精灯把氢氧化钠加热到融化,再电解,通电几分钟后会出现钠金属。用小勺挖出来。

第二种:加热氢化钠。铁坩埚,盖上盖子,装氢化钠,用喷枪加热,几分钟后有钠金属。
第三种:用锂金属置换氢氧化钠或者氯化钠里面的钠。用喷枪加热,几分钟后有融化的钠金属,把坩埚里面的固体倒进有液态石蜡和水的烧杯里,钠会浮出到水面。
第四种:用镁置换氢氧化钠。坩埚里底下放上氢氧化钠,上面放镁粒。喷枪加热几十秒,出现钠金属后同第三种。
以上内容参考:
如何制氢氧化钠溶液
要电解表面潮解的氢氧化钠固体,用铁片作阴极和阳极,分开插入氢氧化钠固体中,
连接直流电源(用摩托车蓄电池),电源电压为24伏,如果接触良好,过一会就可以看到钠固体了。
(注意固体应该放在绝缘且比较耐热耐碱腐蚀的容器中,如瓷器。)
钠的制取及保存的方法有哪些
制取:工业上采用铁粉和高温氢氧化钠反应的方法制备金属钠,同时得到四氧化三铁和氢。电解氢氧化钠也得到金属钠,方程式为:
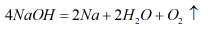
,但是此方法使用较少。
当前工业上普遍采用氯化钠-氯化钙熔盐电解法制金属钠,方程式为:
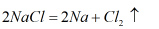
保存方法:
浸放于液体石蜡、矿物油和苯系物中密封保存,大量通常储存在铁桶中充氩气密封保存。金属钠不能保存在煤油中是因为与煤油中的有机酸等物质反应成有机酸钠等物质(呈黄色)附着在钠表面 。当保存在石蜡油中时,空气中的氧气也会进入石蜡油,使金属钠的表面变灰,形成氧化物膜。
钠是一种金属元素,在周期表中位于第3周期、第IA族,是碱金属元素的代表,质地柔软,能与水反应生成氢氧化钠,放出氢气,化学性质较活泼。钠元素以盐的形式广泛的分布于陆地和海洋中,钠也是人体肌肉组织和神经组织中的重要成分之一。
性质:
钠的化学性质很活泼,常温和加热时分别与氧气化合,和水剧烈反应,量大时发生爆炸。钠还能在二氧化碳中燃烧,和低元醇反应产生氢气,和电离能力很弱的液氨也能反应。
应用:
1、工业用途:测定有机物中的氯;还原和氢化有机化合物;检验有机物中的氮、硫、氟;去除有机溶剂(苯、烃、醚)中的水分;除去烃中的氧、碘或氢碘酸等杂质;制备钠汞齐、醇化钠、纯氢氧化钠、过氧化钠、氨基钠、合金、钠灯、光电池,制取活泼金属。
2、生理作用:
钠是人体中一种重要无机元素,在人体中具有十分重要的作用。
(1)钠是细胞外液中带正电的主要离子,参与水的代谢,保证体内水的平衡,调节体内水分与渗透压;
(2)维持体内酸和碱的平衡;
(3)是胰液、胆汁、汗和泪水的组成成分;
(4)钠对ATP(腺嘌呤核苷三磷酸)的生产和利用、肌肉运动、心血管功能、能量代谢都有关系,此外,糖代谢、氧的利用也需有钠的参与;
(5)维持血压正常;
(6)增强神经肌肉兴奋性。
家庭小型实验室怎样制取金属钠溶液
材料:铁皮(约100平方厘米)、铁丝(用回形针拉直)、低压直流电源(约6~15伏),有塑料盖的玻璃瓶。 药品:干燥的片状或块状氢氧化钠固体,煤油或者液体石蜡。 方法:1、将块状氢氧化钠放在铁片中央(片状需要堆叠起来),插入铁丝。 2、铁丝连接电源正极,铁片连接电源负极。 3、通电,反应开始,阳极析出水和氧气,阴极析出金属钠。 +)4OH- -4e-=2 H2O+O2↑ -)Na+ + e-=Na 钠会顺铁片滚出,滚出时可能发生燃烧,可以用干燥的铝箔盖灭。 用小刀刮取钠球,放在装有煤油或者液体石蜡的玻璃瓶中保存。
NaCl在固态时不导电,在融溶状态和水溶液下可以导电,如果是点解水溶液,点解出来就和水反应了,所以只能在融溶状态下点解。
以上就是关于钠怎么家中制取,制取钠单质的化学方程式的全部内容,以及钠怎么家中制取的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【易百科】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。










