AlCl3为什么不是离子化合物
并不是所有的酸、碱、盐离子化合物共价化合物构成粒子阴、阳离子分子或原子离子间的作用离子键分子或原子之间存在的共价键熔沸点较高一般较低,少部分很高导电。
是由阴离子(Anion,带负电)和阳离子(Cation,带正电)组成,以本质上是库仑力的离子键相结合的化合物。
离子化合物通常熔点和沸点较高,熔融时或电离产生其组成离子的水溶液中时能导电。
大部分离子化合物在常温下是固体,但也有一些常温下存在于液态离子化合物,它们通常是一些含有复杂有机组份的盐。
注意液态离子化合物和离子化合物溶液的区别,后者中含有一些不具电性的分子。
alcl3是离子化合物还是共价化合物
Al3+半径相对同周期金属元素简单阳离子来说比较小,净电荷数大,无法和Cl-形成稳定的典型的离子键AL-Cl键仍是共价键.因此氯化铝不是离子化合物,而是共价化合物.
为什么氯化铝不是离子化合物而是共价化合物
因为离子化合物是由阳离子和阴离子构成的化合物,而氯化铝是共价化合物。
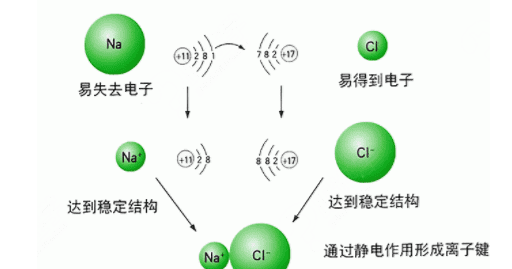
活泼金属(如钠、钾、钙、镁等)与活泼非金属(如氟、氯、氧、硫等)相互化合时,活泼金属失去电子形成带正电荷的阳离子(如Na+、K+、Ca2+、Mg2+等),活泼非金属得到电子形成带负电荷的阴离子(如F-、Cl-、O2-、S2-等),阳离子和阴离子靠静电作用形成了离子化合物。
例如,氯化钠即是由带正电的钠离子(Na+)和带负电的氯离子(Cl-)构成的离子化合物。在离子化合物里阳离子所带的正电荷总数等于阴离子所带的负电荷总数,整个化合物呈电中性。
扩展资料:
离子化合物(ionic compound)是存在于:
1、活泼金属(指第一和第二主族的金属元素)与活泼的非金属元素(指第六和第七主族的元素)之间形成的化合物
2、金属元素与酸根离子之间形成的化合物。(酸根离子如硫酸根离子SO₄²-、硝酸根离子NO3-、碳酸根离子CO₃²-等等);
3、铵根离子(NH4+)和酸根离子之间,或铵根离子与非金属元素之间,例如NH4Cl、NH4NO3。
4、NaH,KH等活泼金属氢化物。
离子化合物都是电解质。在熔融状态下:都可以导电(此类物质加热时易分解或易氧化)。在水中:有的可以导电,有的不可以导电(此类物质易与水反应或不溶于水)。 在原电池中的作用:形成闭合电路。
氯化铝为什么不是离子化合物?
因为离子化合物是由阳离子和阴离子构成的化合物,而氯化铝是共价化合物。铝离子所带电荷数大,离子半径小,有很强的极化能力,而氯离子半径较大,极化率很大,容易变形,故两者结合发生极化作用,离子键极化为共价键,所以氯化铝是共价化合物。
氯化铝的用途
1.用作有机合成的催化剂,如石油裂解、合成染料、合成橡胶、合成洗涤剂、医药、香料等;
2.用于制造农药、有机铝化合物、酞菁系有机颜料用催化剂、乙基苯制造用催化剂;
3.用于金属冶炼、润滑油合成;
4.食品级产品用作膨松剂、清酒等防变色剂及果胶的絮凝剂;
5.用作分析试剂、防腐剂、媒染剂。
H2为什么不是共价化合物
氯化铝中氯和铝是以共价键方式结合,而非离子键,因此AlCl3是共价化合物而不是离子化合物。
有金属离子和非金属离子并不一定是离子化合物,如氯化铁等。
氯化铝:
氯化铝,或三氯化铝,化学式为AlCl3,是氯和铝的化合物。氯化铝熔点、沸点都很低,且会升华,为有离子性的共价化合物。熔化的氯化铝不易导电,和大多数含卤素离子的盐类(如氯化钠)不同。
英文名:Aluminum
chloride
别
称:三氯化铝
化学式:AlCl3
分子量:133.34
熔
点:190
°C
(463
K
2.5
大气压)
沸
点:178
°C
(451
K)
(升华)
水溶性:易溶
密
度:2.48
外
观:无色透明或浅黄色的结晶性粉末
摩尔质量:133.34g/mol
参考:
以上就是关于AlCl3为什么不是离子化合物的全部内容,以及AlCl3为什么不是离子化合物的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【易百科】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。




