怎么样判断离子半径的大小呢
对于同一周期的金属元素,质子数越大,离子半径越小。因为同一周期的元素离子外面的电子层数是相同的。一般离子比较大小都比较金属离子的大小。
离子是指原子由于自身或外界的作用而失去或得到一个或几个电子使其达到最外层电子数为8个或2个(氦原子)或没有电子(四中子)的稳定结构。
如何判断离子半径的大小?
要依次三看:
一看电子层数,大的半径大电子层数相同时。
二看核电荷数,小的半径大电子层数相同且核电荷数相同时。
三看最外层电子数,多的半径大如氯离子半径大于氯原子我还是老师的时候就教学生这样记忆,比其他书上好几条的要好多了。
离子半径:
1、电子层数相同的离子,根据其核电核数大小判断:核电核数多的离子半径小,核电核数少的离子半径大;
2、电子层数不同的离子,根据电子层数判断:电子层数多的离子半径大,电子层数少的离子半径小。
原子半径:
1、如果在同一周期,则原子序数越大,半径越小。
2、如果不是同一周期,则周期越大则半经越大。
3、对一同一原子,阴离子半经〉原子半经〉大于阳里子半经。
4、对于电子数相同的,原子层数多,则半经小.如钠理子〈氟理子)。
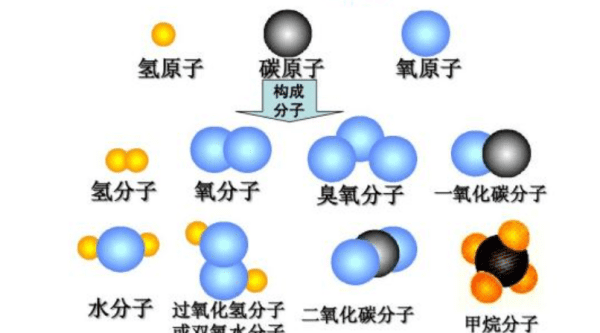
扩展资料
原子、离子半径大小解析:
要比较微粒半径的大小,可以根据元素间在元素周期表中的位置来判断,它们的判断口诀为:同层核大半径小,同族核大半径大。
但是,这个口诀只能针对原子半径大小的比较,对于其它微粒,比如离子等的比较则无能为力.对于其它微粒的比较,我们只要按照以下顺序操作即可(注意:需在可以比较的情况下)。
①电子层数.电子层数多,半径大.可以这样理解,电子在原子核外按层排布,类似于洋葱,皮(层)多,洋葱(原子)的半径自然就大。
②如果电子层数相同,则比较核电荷数,核电荷多,则半径小.电子层相同时,核电荷越多,原子核对核外电子的吸引力越大,原子核自然将电子的距离拉的更近。)
③如果电子层数还是相同时,则比较电子数,电子数多,半径大(形象记忆:多"吃"了一个电子,则长胖了!电子和电子之间存在一个排斥作用力,电子越多,相互之间的排斥越强烈,自然要占据更大的空间)。
如何比较离子半径大小?
比较离子半径大小的方法:
1、电子层数。电子层数多,半径大。可以这样理解,电子在原子核外按层排布,类似于洋葱,皮(层)多,洋葱(原子)的半径自然就大。
2、如果电子层数相同,则比较核电荷数,核电荷多,则半径小。
3、如果电子层数还是相同时,则比较电子数,电子数多,半径大。
离子半径是描述离子大小的参数。取决于离子所带电荷、电子分布和晶体结构型式。设r阳为阳离子半径,r阴为阴离子半径。r阳+r阴=键长。r阳/r阴与晶体类型有关。可从键长计算离子半径。一般采用Goldschmidt半径和Pauling半径,皆是NaCl型结构配位数为6的数据。Shannon考虑了配位数和电子自旋状态的影响,得到两套最新数据,其中一套数据,参考电子云密度图,阳离子半径比传统数据大14pm,阴离子小14pm,更接近晶体实际。
怎样比较简单离子半径的大小
(1)阳离子半径小于相应的原子半径如
(2)阴离子半径大于相应的原子半径。
(3)同种元素不同价态的离子,价态越高,离子半径越小。
(4)电子层结构相同的不同粒子,其半径比较的规律是:核电荷数越大,半径越小。
参考资料:
化学强人如何判断离子半径大小的方法
离子半径大小1.同周期:分金属离子和非金属离子,若是金属离子与非金属离子比较,金属离子的半径小于非金属离子,若是金属离子与金属离子或非金属离子与非金属离子比较则原子序数大的半近小
2.同族,电子层数越多半径越大即族数越大半径大
3.电子层数相同时,原子序数大的半径小
首先OF是同一周期的非金属离子,故氧离子半径大于氟离子
NaMgAl是同一周期的金属离子,故钠离子的半径最大,铝离子的半径最小,
Ne是稀有气体,而稀有气体一般都是单原子分子,在同一周期中,稀有气体原子半径是最大的
所以离子顺序是O>F>NA>MG>AL
以上就是关于如何判断离子半径的大小,怎么样判断离子半径的大小的全部内容,以及怎么样判断离子半径的大小呢的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【易百科】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。