溴苯和苯为什么不能用水分离
因为溴苯和苯都难溶于水。而且溴苯溶解于苯中。溴苯是一种苯的卤代物。无色至淡黄色澄清液体,有特殊的芳香气味。化工上主要用于溶剂、分析试剂和有机合成等。
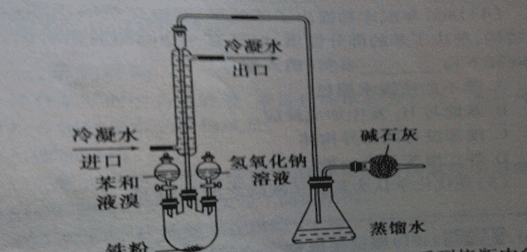
溴苯由苯与溴反应而得。先将铁粉和苯加入反应器,在搅拌下慢慢加入液溴,加完后于70-80℃保温反应1h,所得粗品用水及5%氢氧化钠溶液洗涤,静置分层,蒸馏;干燥;过滤,最后经常压分馏,取155-157℃馏分而得成品。
除去溴苯中的苯为什么不能加水分液
因为溴苯和溴在水中的溶解度都不是很大 而且溴和溴苯互溶 你向溴和溴苯德混合液中加水 只会分为两层 水层和有机层 ;溴苯的熔沸点比苯的熔沸点低,所以应该蒸馏出沸点低的 留下沸点高的溴苯.
为什么苯和溴苯不能用水分离出来
A 苯和溴苯的沸点相差较大,蒸馏即可实现分离,A正确。氨气和氯化氢极易溶于水,导管口不能直接插入到溶液中,否则会导致倒吸,B不正确。氯化铵分解产生氯化氢和氨气,但温度降低后,两种气体又反应生成氯化铵,C不正确。CO 2 的密度大于空气的,应该是长口进入,NO极易被氧化,所以不能用排气法收集,D不正确,答案选A。
加水可以分离苯和溴苯
前几天就看到这个问题了,但我看到好多同学用计算、用相图来回答了,感觉已经相对完备,因为这些是化学学科的基石,没想到这会儿又争议起来了。还有同学引用高同学的实验调侃计算化学不准确,这个我想说,计算化学不准指的多是分子间作用、反应动力学等等这些方面不准,这种热力学方面的东西,还是能顶用的。我跟高同学也讨论了,我认为他的实验所看到的分层并不是真正意义上的分层,而是有些液体粘附在玻璃上面导致的,这也是因为他做的量比较小,表面张力的影响比较显著。所以今天,我特地做一个量大一点的给大家看一下首先原料略有不同,因甲苯是管制品,用二甲苯替代,溴苯不是很常用,用氯苯替代。在100毫升的量筒中加入30毫升氯苯,这个数量可以说表面张力已经不能起到扭转乾坤的作用了。 然后加入30毫升水(加了少许水溶性颜料,以方便观察) 然后再小心地用滴管滴加30毫升二甲苯这个时候可以看到,因为密度的差别,它们分成了三层。接下来用用滴管将量筒内的液体混合。然后静置。可以看到,水相逐渐下沉。过了很长时间以后,水相已经基本完全沉底,体系分成两相,两相,两相,但仍然有一些水滴吸附在玻璃上。仔细观察,可以发现油水界面上也有很水液滴最终没有聚并在一起。可见即使用了100毫升这么多,也没法完全避免水滴吸附在玻璃表面上。但总体上已经影响不大了,至少不会误判有几相。
关于高中有机化学的知识点
苯和溴苯原来是互溶的,加入水后,都要受到H2O的浮力。
其中苯受的浮力大于重力(因为苯比水轻),溴苯则重力大于浮力,两者被迫居于水层的上下两侧,不再接触,所以会分层。并且溴的溶解度在溴苯中更大 所以是含溴的溴苯
两个密度不同的有机物加水分离,有两个要求:一是均难溶于水,二是密度一个比水大另一个比水小。
苯和溴苯正常情况下是互溶的没错 如果要二者分离首先想到的一般是蒸馏
分液其实也可以 只不过效果不如蒸馏
希望对你有帮助 不懂欢迎追问
以上就是关于溴苯和苯为什么不能用水分离,除去溴苯中的苯为什么不能加水分液的全部内容,以及溴苯和苯为什么不能用水分离的相关内容,希望能够帮到您。
版权声明:本文来自用户投稿,不代表【易百科】立场,本平台所发表的文章、图片属于原权利人所有,因客观原因,或会存在不当使用的情况,非恶意侵犯原权利人相关权益,敬请相关权利人谅解并与我们联系(邮箱:350149276@qq.com)我们将及时处理,共同维护良好的网络创作环境。



